联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
DNA损伤应答(DDR)缺陷引发的基因组不稳定性是癌症的核心特征与重要治疗靶点,针对该过程的靶向治疗策略,成为当前肿瘤治疗的研究热点。作为DDR的关键调控因子,双特异性酪氨酸磷酸化调节激酶(DYRK)家族在肿瘤发生及治疗响应中的具体机制尚待阐明。深入理解DYRK与DDR的功能互作,深化对该激酶家族的认知,将为DYRK抑制剂的开发及精准肿瘤学策略提供理论支撑和重要依据。
山东大学董超研究员团队长期致力于DNA损伤修复与基因组稳定性调控机制、胃肠道疾病的研究。近日,该团队在本刊发表了题为“Emerging roles of DYRK-mediated DNA damage response in cancer”的综述文章。该综述系统梳理了DYRK介导DDR信号转导及影响癌症进程的机制,***评估了DYRK抑制剂的研发进展与临床潜力。
DYRK家族激酶是进化上高度保守的CMGC家族成员,作为细胞生理活动的多效调节因子,协调包括细胞增殖、凋亡及肿瘤干细胞维持在内的多种生物学过程(图1)。这些激酶广泛参与调控细胞周期动力学、DNA修复机制及转录程序,凸显了其在肿瘤发生发展与基因组不稳定性中的关键作用。 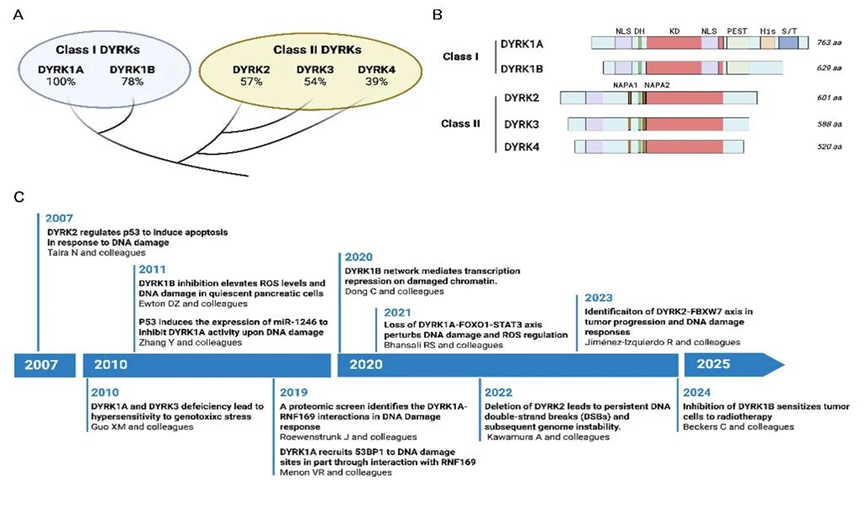
图1 DYRK激酶参与DNA损伤应答的关键里程碑事件(原文Figure 1)
DYRK家族激酶通过整合DNA损伤诱导的信号级联反应,与已知DDR调控蛋白相互作用,协调各类DDR通路以决定细胞命运,特别是在程序性细胞死亡的启动中发挥关键调控作用(图2)。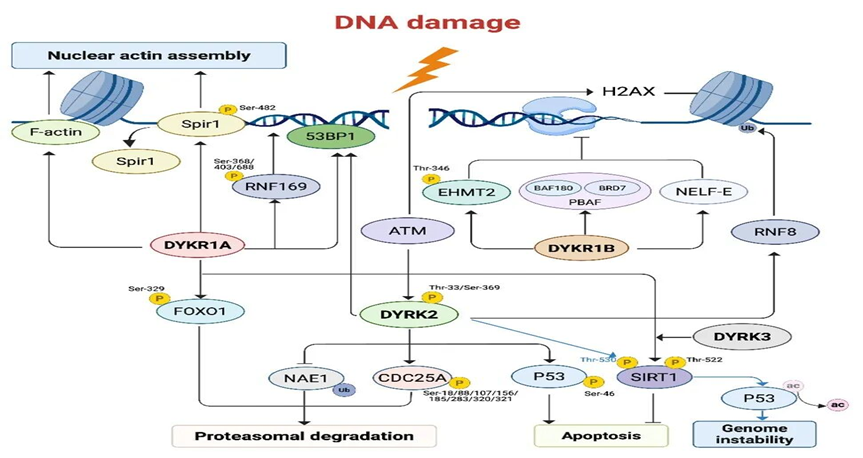
图2DYRK激酶参与细胞DNA损伤应答调控的分子机制示意图(原文Figure 3)
作为免疫稳态的重要决定因素,DYRK激酶为肿瘤治疗开辟了新路径。这些激酶展现出广泛的调控谱系,其功能活性显著依赖性于免疫微环境。DYRK激酶在肿瘤治疗中***潜力,主要源于其抑制剂独特的双重功效:既能直接抑制癌细胞存活,又能有效重编程免疫抑制性肿瘤微环境(TME)(图3)。因此,DYRK激酶构成了***价值的多功能靶点,通过“内源性削弱癌细胞活力、外源性激活抗肿瘤免疫”的双重策略发挥抗癌作用。
RNA提取磁珠属于纳米生物磁珠的一种,主要作用是用于核酸提取过程中的RNA提取,粒径分布在500nm左右,是洛阳吉恩特生物自主研发生产的高分子纳米磁性微球,该磁珠悬浮时间长,磁响应时间迅速,对DNA甲基化过程中的提取环节提供良好的支持,可明显缩短实验时间,提高实验效率,并在提取结果上保持稳定,配合核酸提取仪,更能实现快速的RNA提取。