联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
导 读:胃癌具有高度的瘤内异质性,因此想要通过解剖学、分子生物学或者细胞培养等方法准确地评估胃癌患者的化疗效果,准确性都有待提高。
近日,北京大学肿瘤医院的研究人员采集和分析了晚期胃癌患者在接受药物治疗期间,个体内ctDNA(循环肿瘤DNA)的基因组变化指标,以探究ctDNA的基因组不稳定水平变化能否用于监测晚期胃癌的药物治疗进展。

染色体加倍或出现异常,是细胞癌变的特征指标,也是恶性肿瘤异常增殖的“罪魁祸首”。因此,在染色体水平上对循环肿瘤细胞进行鉴定评估,可以准确判断肿瘤状态以及患者的治疗进展。然而,鉴于不同种类肿瘤的染色体变化也不同,所以对肿瘤疗效评估的研究也参差不齐。
其中,针对胃癌的染色体评估尤为困难。一方面,胃癌原发于空腔脏器,易发生腹膜转移,因此通过现有影像学的评价标准,难以准确评估;另一方面,胃癌患者的肿瘤异质性差异明显,且肿瘤微环境十分复杂,因此常规的染色体或分子水平的评估手段都比较困难。综合来看,针对胃癌设计更有效的疗效评估方法刻不容缓。
有研究发现,ctDNA—即肿瘤细胞的DNA经脱落或细胞凋亡后进入循环系统,可以作为一种特征性的肿瘤生物标记物。因此,通过检测ctDNA,能够准确追踪血液中的肿瘤去向。
同时,研究人员发现,ctDNA的基因组不稳定性变化还可预测化疗或免疫治疗对多种恶性肿瘤的疗效。但是,这套评估标准对“老大难”的胃癌,是否还行之有效呢?
对此,北京大学肿瘤医院的研究人员收集了55例晚期胃癌(AGC)患者化疗/靶向治疗前的血浆样本,以及26例晚期胃癌患者化疗/靶向治疗中的血细胞样本,经过分离提取血浆中的ctDNA,再通过全基因组测序(WGS) 评估各样本中体细胞拷贝数变异度(SCNA),并计算分析全基因组染色体的不稳定性评分(CNI)与治疗反应之间的相关性。
研究结果发现,在55例AGC治疗前的病例中,有27例(49%)在药物治疗前出现了染色体不稳定性,其对药物治疗的缓解率为59%(16/27),这明显高于治疗前染色体稳定的患者数量(32%,9/28,P = 0.043)。
此外,研究人员还发现, 共有26例患者的CNI评分在治疗期间出现了波动。其中93%(14/15)的患者在接受治疗后,表现为药物治疗敏感,且体内ctDNA的基因组不稳定评分明显下降,而52%(13/25)的患者中ctDNA具有治疗耐药性,并且显示高水平的基因组不稳定评分。而对于具有耐药性的ctDNA来说,其SCNA指标在治疗前和治疗后均不变,而治疗后的CNI评分则低于治疗前。
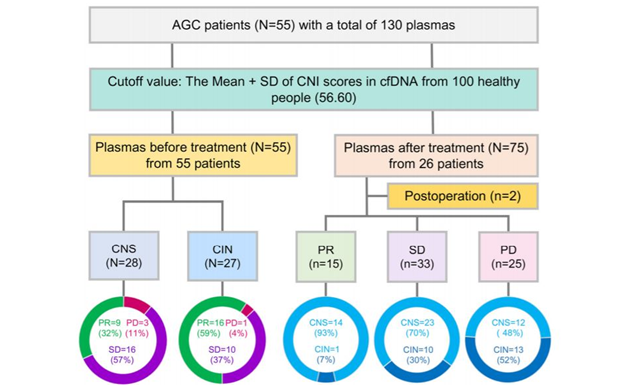
130份血浆样本的示意图和55名病例的的治疗进展
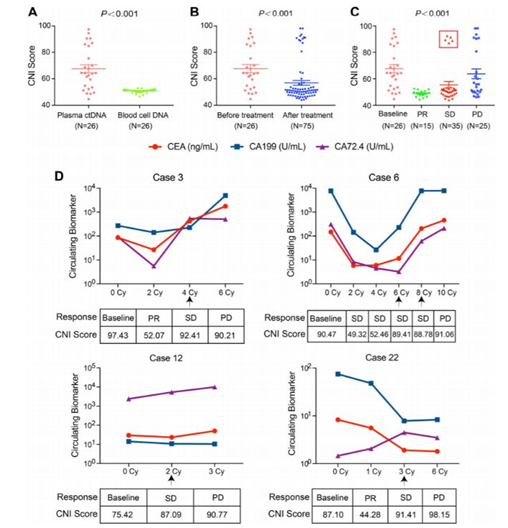
26例血浆样本中ctDNA的CNI评分动态变化
这项研究通过低覆盖度WGS技术对晚期胃癌患者血浆中ctDNA的染色体不稳定性进行了定量分析,揭示了AGC药物治疗引起的CNI评分的动态变化,为准确监测胃癌的靶向治疗效果提供了可行方案。
结果表明,ctDNA的染色体不稳定性可预测和监测晚期胃癌患者的用药效果,但这一评估标准仍需要通过大数据进一步验证。
G.N.T.生物磁珠有着稳定的技术参数,良好的悬浮性,可靠的吸附性,用量和性价比都普遍适合各种生物实验室使用。配合磁珠法核酸提取试剂盒,不论是进行课题研究,还是产品生产,都是很好的选择。能够有效地从生物样本,如血液、组织、拭子中提取到纯度合理的核酸。对下游的检测和测定,有着良好的基础适应性,能够广泛应用于生物实验室的各种分子实验。这一过程可以在仪器的作用下自动化高通量地进行,大大节省了时间,提高了效率。且如果是对病原生物样本进行提取纯化,可以通过仪器提取,进行与操作人员的安全隔离。对于基因相关研究都有着重要意义。深受相关实验室好评。
参考文献:
Zuhua Chen, Cheng Zhang, et al. Chromosomal instability of circulating tumor DNA reflect therapeutic responses in advanced gastric cancer. Cell Death & Diseasevolume 10, Article number: 697 (2019)